Au milieu des années 1990, apparaissent les premiers médicaments laissant entrevoir la possibilité, pour les malades du SIDA, de retrouver une espérance de vie normale : les inhibiteurs de la protéase. Parmi ceux-ci, le ritonavir est l’un des premiers brevetés. Encore utilisé aujourd’hui, il est présent sur la liste modèle de l’OMS des médicaments essentiels, et est prescrit contre le VIH, ou le SARS-CoV-2, en combinaison d’un autre antiviral dont il vient augmenter l’efficacité.
Pourtant, il a bien failli disparaître.
Le VIH, le SIDA, et les inhibiteurs de la protéase
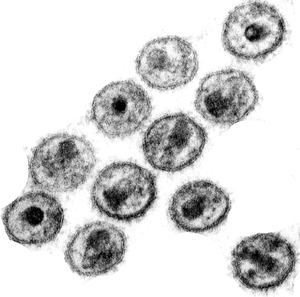
Le VIH vu au microscope
Le SIDA (pour Syndrome d’ImmunoDéficience Acquise) est le nom donné à l’ensemble de symptômes qui apparaissent lors du dernier stade de la maladie causée par l’infection par le virus de l’immunodéficience humaine (VIH). Le VIH serait apparu il y a un siècle, à Léopoldville, capitale du Congo Belge (aujourd’hui Kinshasa, capitale de la République Démocratique du Congo). Un demi-siècle plus tard – et sans que l’on ne sache vraiment comment, le virus s’est propagé. Les premiers foyers de contamination par le VIH apparaissent aux États-Unis et en Europe dans les années 1970, mais les symptômes n’en sont pas encore identifiés. La maladie couve, et cinq ans plus tard, alors que les symptômes apparaissent chez un nombre grandissant de personnes, le VIH (dont on ignore encore l’existence), commence à devenir un sujet de santé publique. En 1980 le premier patient de l’épidémie américaine est diagnostiqué. En 1982, la maladie est officiellement baptisée SIDA, la même année, le premier patient français est diagnostiqué. Un an plus tard, en 1983, une équipe de l’institut Pasteur découvre le virus responsable, découverte pour laquelle Luc Montagnier et Françoise Barré-Sinoussi recevront le prix Nobel de médecine en 2008. En 1986, le virus est baptisé VIH.
Les premiers médicaments contre le VIH arrivent en 1987, mais sont peu efficaces. Le pronostic est alors encore sombre pour qui apprend être infecté. En 1992, soit dix ans après la découverte du virus, ce sont plus de 100 000 personnes1 qui sont mortes du SIDA aux États-Unis. L’épidémie fait rage. À San Francisco, Los Angeles, et New York, c’est la première cause de mort chez les jeunes hommes1. En France, au plus fort de l’épidémie, en 1994, près de 6 000 personnes sont mortes en un an2.
En 1995, une quinzaine d’années après les premiers cas détectés dans le monde occidental, une révolution pharmacologique se produit. Une nouvelle famille de médicaments fait son apparition: les inhibiteurs de la protéase. Ces nouvelles molécules, combinées à d’autres médicaments antiviraux, font figure de miracle. En deux ans, le nombre de décès liés au VIH a été réduit de deux tiers aux États-Unis.
Chiffres du VIH/SIDA de 1981 à 2009 aux États-Unis. On remarque juste après l'introduction des nouveaux traitements une diminution nette du nombre de décès annuels liés à la maladie, tandis que le nombre de personnes malades du SIDA augmente alors que le nombre de nouveaux diagnostics baisse, traduisant l'allongement notable de l'espérance de vie des malades.
Neutraliser le Cytochrome P450 3A4
Formule topologique du ritonavir
Ces nouveaux médicaments, ces inhibiteurs de la protéase, agissent en empêchant l’action d’une enzyme3 nommée protéase. Cette enzyme est essentielle au VIH à qui elle permet de se répliquer. Inhiber la protéase, c’est donc empêcher la reproduction du virus. Malheureusement, nombre de ces inhibiteurs de la protéase partagent un point faible : ils sont détruits, au niveau de notre foie, par une autre enzyme – humaine celle-ci : le cytochrome P450 3A4. Cette destruction par le cytochrome P450 3A4 fait que seule une faible part des doses de médicament prises par le patient arrive au virus et l’attaque. Pour compenser, il faut prescrire des doses plus élevées, qui sont moins bien tolérées car elles entraînent plus d’effets secondaires, et forcent à des prises plus fréquentes et contraignantes. Enfin, la faiblesse de la quantité de médicament qui agit in fine sur le virus peut entraîner l’apparition de souches du VIH qui résistent au traitement.
Et pourtant, le miracle de 1995 s’est bien produit, et les inhibiteurs de la protéase ont permis de mettre en place des thérapies d’une efficacité alors jamais vue, en dépit de leur dégradation par le cytochrome P450 3A4. Ce miracle, on le doit en partie à l’un de ces inhibiteurs de la protéase en particulier: le ritonavir. En effet, si le ritonavir inhibe bien la protéase, il inhibe surtout le cytochrome P450 3A4. Il est donc couramment combiné à d’autres molécules – plus efficaces que lui contre le VIH – qu’il protège de l’action du cytochrome P450 3A4, et dont il permet de décupler l’effet contre le VIH sans devoir augmenter la dose prescrite, limitant ainsi les effets secondaires terribles, qui poussaient certains patients à préférer arrêter leur traitement.
Ainsi le ritonavir fût le fer de lance de la révolution thérapeutique des années 1995 et permis de redonner espoir aux 800 000 personnes qui vivaient alors avec le VIH. Mais en 1998, c’est la catastrophe : le ritonavir est retiré du marché.
Cristaux

Un cristal de calcite
Le ritonavir était initialement vendu sous forme d’un comprimé, fabriqué à partir d’une poudre composée de cristaux de ritonavir. Nombre de médicaments sont en fait commercialisés sous forme de microscopiques cristaux. Un cristal est un matériau solide, qui a la particularité que les molécules qui le constituent sont arrangées régulièrement, et que leur arrangement est constitué de la répétition d’un même motif de base, appelé la maille du cristal.
Les cristaux de ritonavir, par exemple, se forment à partir d’une solution contenant la molécule dissoute en grande concentration. Spontanément, des minuscules cristaux vont apparaître dans cette solution. C’est la germination, ou nucléation. Sur ces “germes”, du ritonavir va continuer à se déposer, faisant ainsi peu à peu grandir le cristal. En se déposant, le ritonavir va adopter la même organisation que le cristal qu’il rejoint, un peu comme l’on continuerait à poser du parquet ou des tomettes en ne pouvant que prolonger et répéter le motif déjà entamé.
Un cristal se forme à partir d'une ▒ solution dans laquelle un █ “germe” apparaît spontanément. Autour de ce noyau, █ le cristal grandit.
Ce phénomène est aussi celui utilisé dans les marais salants : l’évaporation de l’eau de mer fait augmenter la concentration du sel qui cristallise. D’autres cristaux se forment différemment : à partir d’un liquide qui refroidit (la glace, les roches issues du magma) ou même à partir d’autre solides dans certaines conditions de température et de pression. Que le cristal soit issu d’une évaporation, d’un refroidissement ou d’un autre processus physico-chimique, la manière dont ses molécules se sont arrangées lors de la cristallisation est déterminante. Sur les quatres images ci-dessous, on peut par exemple voir quatre cristaux différents. Pourtant, il n’y a en tout que deux espèces chimiques représentées. Ces cristaux vont donc de paire : deux d’entre eux sont composés de carbone pur, et les deux autres de carbonate de Calcium (CaCO3). Saurez-vous deviner lesquels ?
Réponse
Le diamant et le graphite ont la même composition chimique (du carbone pur), tandis que la calcite et l'aragonite sont tous deux composés de carbonate de calcium. Par exemple, le diamant par exemple est composé d'atomes de carbone arrangés en sorte de doubles cubes imbriqués, tandis que le graphite est constitué de feuilles plates d'atomes de carbone.

Diamant

Aragonite

Graphite

Calcite
Différents cristaux. Parmi eux, certains ont la même composition chimique, saurez-vous deviner lesquels ?
Ces différentes formes possibles de la structure cristalline d’un même composé chimique sont appelées des polymorphes. Deux polymorphes différents, bien qu’ayant rigoureusement la même formule chimique peuvent avoir des propriétés radicalement différentes. Essayez donc de lire vos vinyls avec une pointe en graphite ou de remplacer la mine de votre crayon à papier par un diamant. Pourtant, les deux sont du carbone pur.
Les facteurs qui entrent en jeu pour déterminer quel polymorphe est formé sont multiples, variés, et incluent la température, la pression, la concentration de la solution à partir de laquelle est formé le cristal, etc. Néanmoins, autour d’un germe d’un certain polymorphe ne va pousser en général qu’un cristal du polymorphe lui-même.
Et c’est là tout le problème.
La forme seconde du ritonavir

Un microscope
Lorsque le ritonavir est mis sur le marché en 1995, il l’est sous une forme cristalline particulière. Les chimistes étant de grands créatifs, cette forme fût poétiquement baptisée Forme I. En 1998 cependant, plusieurs lots successifs de ritonavir échouent à passer le test de qualité du fabricant : pas assez soluble, le ritonavir produit ne serait pas correctement assimilé par l’organisme. Panique à bord, les lots incriminés sont étudiés, et les résultats de microscopie et de diffraction à poudre sont formels : une seconde forme du ritonavir est spontanément apparue. Cette seconde forme, baptisée forme II, est du point de vue clinique bien moins intéressante que la première puisque bien moins soluble. Pire encore: elle se répand. La forme II apparaît à de plus en plus d’endroits de la chaîne de production : après quelques semaines, ni la zone de fabrication, ni la zone de conditionnement ne sont épargnées4. Les stocks de ritonavir s’effondrent, et son fabricant est obligé de le retirer du marché le temps de trouver une solution.
Les choses ne se sont pas faites graduellement. Quelque chose s’est passé et a provoqué l’apparition de la nouvelle forme… Il n’y a eu aucun signe avant coureur.
Si la forme II s’est répandue si vite, c’est parce qu’elle est beaucoup plus stable que la forme I. La forme I se forme bien plus fréquemment de manière spontanée, mais se transforme naturellement en la forme II si elle y est exposée, et il suffit pour cela d’un germe minuscule. Ainsi, on considère que quelques millions de molécules suffisent à initier la transformation. Si ce nombre peut paraître grand, il faut le remettre en perspective. Imaginez le plus petit cristal possible, qui soit encore visible à l’œil nu. Brisez-le en un milliard de cristaux encore plus petits. Chacun de ces cristaux suffirait à initier la transformation de la forme I en la forme II.
Une fois que la forme II était introduite dans un laboratoire, il devenait impossible de l’en débarrasser de ses résidus microscopiques, et donc impossible d’y produire la forme I. Certains ont même émis l’hypothèse qu’un employé qui entrerait une seule fois en contact avec la forme II aurait pu ensuite empêcher la production de la forme I par sa seule présence.5
Nous avons tout essayé. Nous avons mené d’innombrables expériences. Nous avons remis à neuf nos installations. Nous avons reconstruit des installations et de nouvelles lignes de production. Nous avons étudié d’autres sites. Nous avons rendu visite à un certain nombre d’[autres] organisations dans le monde… pour voir si nous pouvions faire quelque chose… pour voir si nous pouvions repartir sur de bonnes bases dans un nouvel environnement sans la forme II.
Finalement, une formulation pharmaceutique différente du ritonavir fût proposée, et l’on identifia des conditions qui empêchaient l’apparition de la forme II. En 1999, le médicament est à nouveau sur le marché, mais son fabricant a entre-temps perdu 250 millions de dollars, et l’ampleur de la crise transparaît dans les déclarations de ses dirigeants (citées au long de cette partie).
…nos actions initiales avaient pour but d’éliminer la forme II de notre environnement. Puis nous nous sommes rendus à l’évidence que nous ne pouvions nous débarrasser de la forme II. Nos actions suivantes eurent pour but de chercher à savoir comment vivre dans un monde de forme II.
Les polymorphes menacés
Une proposition de drapeau pour la Terre
Au-delà du cas du ritonavir, le problème posé par l’apparition de nouveaux polymorphes est plus général. Étant donné qu’un germe minuscule peut suffire à empêcher la fabrication de certaines formes cristallines, il est probable que certains cristaux soient, à l’échelle de la planète, des espèces définitivement éteintes. Une fois l’atmosphère de notre planète chargée d’infimes poussières de la forme la plus stable du polymorphe, celles-ci contamineront et transformeront les polymorphes moins stables, menant à leur disparition.
C’est par exemple ce qui est arrivé à la progestérone. Les premiers scientifiques ayant travaillé sur cette hormone utilisée comme médicament décrivent être capable d’en synthétiser deux formes, nommées I et II, et de transformer la II en la I. Pourtant, à partir du milieu des années I970, il devient impossible de synthétiser la forme II. Même en suivant les protocoles de leur prédécesseurs, les chercheurs aboutissent inévitablement à la forme I. L’une des théories avancées pour expliquer ce phénomène est que les cristaux de forme I, plus stables, se seraient répandus de l’atmosphère, et “ensemenceraient” toute solution de progestérone, empêchant les cristaux de forme II d’apparaître.
L’extinction des génériques
Enfin, l’extinction de certains polymorphes se retrouve intimement liée à des procès de propriété intellectuelle. Prenons l’exemple de la paroxétine (vendue sous le nom de Paxil, Deroxat ou Seroxat). En 1980, Beecham (une filiale de GSK) acquiert les droits de cette molécule découverte dans les années 1970s afin d’en faire un médicament. La seule forme connue est alors la forme II (le nom lui fût donné après). En 1984, une nouvelle forme (la I) apparaît spontanément dans deux usines de Beecham. En 1986, Beecham dépose une demande de brevet pour cette nouvelle forme, brevet qu’elle obtient en 1988. En 1993, la molécule est mise sur le marché. Dans le cas de la paroxétine, c’est la forme I qui est la plus stable, et dont d’infimes poussières peuvent transformer (dans certaines conditions) la forme II.
En 1998, une demande est déposée par Apotex pour obtenir le droit de commercialiser une version générique de la paroxétine sous sa forme la plus ancienne (la forme II) dont le brevet doit expirer en 2006. Mais GSK s’y oppose. Leur argument: les usines d’Apotex sont contaminées par la forme I, plus récente et encore sous brevet, et vont donc produire certes une majorité de forme II mais également – à leur insu – un peu de forme I, et par là enfreindre le brevet. Heureusement, le juge chargé de l’affaire donnera raison à Apotex, qui ne pouvait selon lui être considéré responsable de la production involontaire de la forme I.